帶你認識流式細胞術(shù)PART 3
更新時間:2025-12-02
瀏覽次數(shù):265
單細胞樣品制備樣品制備
如果研究對象是體外培養(yǎng)的懸浮細胞,則直接收集細胞于離心管中,離心沉淀細胞,然后PBS清洗重懸沉淀,取適量于EP管中,標(biāo)記染色相應(yīng)的熒光素偶聯(lián)抗體,最后洗去未結(jié)合的抗體,用適宜體積PBS重懸細胞進行上樣;
熒光標(biāo)記
熒光信號是流式細胞儀接受處理的主要信號;
流式細胞儀接收到的熒光信號主要來源于結(jié)合在樣品細胞上的熒光素;
熒光素偶聯(lián)抗體/染料與細胞結(jié)合后就會使細胞帶有相應(yīng)的熒光素,該熒光素被特定波長的激光激發(fā)后產(chǎn)生特定波長范圍的熒光,分析該熒光信號的強弱就可間接反映樣品細胞的某些特征;
熒光素
熒光素大都是一些化學(xué)試劑,有天然的、半天然的,也有人工合成的,有些是蛋白質(zhì)。
熒光素產(chǎn)生熒光原理:熒光素(原子)在未被激發(fā)時外層電子處于基態(tài),當(dāng)被特定波長的激光激發(fā)后,外層電子接收到足夠的能量就會躍遷到激發(fā)態(tài),再回到基態(tài)同時釋放熒光。
熒光素偶聯(lián)抗體
由熒光素和抗體兩部分組成,抗體一般是單克隆抗體。
偶聯(lián)抗體產(chǎn)生熒光原理:在標(biāo)記細胞時,熒光素偶聯(lián)抗體中的抗體能與相應(yīng)的抗原分子特異性結(jié)合,這時細胞表面就順帶結(jié)合了熒光素,同樣被激光激發(fā)后產(chǎn)生熒光。
樣品封閉
有些細胞表面受體會非特異性結(jié)合某些熒光素偶聯(lián)抗體,產(chǎn)生混雜信號,導(dǎo)致流式分析結(jié)果錯誤,所以需要消除這種非特異性結(jié)合的影響。
方法:在熒光素偶聯(lián)抗體標(biāo)記前先封閉樣品細胞。
具體:先用無關(guān)抗體孵育細胞,使細胞表面非特異性受體結(jié)合無關(guān)抗體,再用熒光素偶聯(lián)抗體正常染色,保證所有的結(jié)合都是抗原與熒光素偶聯(lián)抗體的特異性結(jié)合。
熒光素偶聯(lián)抗體的標(biāo)記方法
直接標(biāo)記法:于單細胞懸液中加入適量的熒光素偶聯(lián)抗體(保證熒光素偶聯(lián)抗體與細胞相比相對過量),充分混勻,4℃靜置孵育30min,然后用PBS洗去未結(jié)合的抗體,重懸細胞后就可以上樣分析。
間接標(biāo)記法:先用生物素偶聯(lián)抗體標(biāo)記樣品細胞,再用熒光素偶聯(lián)鏈霉親和素標(biāo)記樣品細胞。此方法一般在多通道分析需要通道搭配以減少熒光素偶聯(lián)抗體的種類時使用。
電壓設(shè)定

目的:使細胞位于流式圖的中心位置,防止細胞群接近邊界而變形扭曲或者處于邊界外;分隔開不同特征的細胞群。
原理:流式細胞儀利用光電倍增管將各通道檢測到的熒光信號轉(zhuǎn)變?yōu)殡娮有盘?,并在轉(zhuǎn)變信號時按照一定比例提高電子信號的強度(提高倍數(shù)可以實時調(diào)控-即調(diào)節(jié)光電倍增管的電壓)。電壓設(shè)置越低,光信號轉(zhuǎn)化時電子信號增強的倍數(shù)越小,得到的電子信號就越弱,反之亦然。
操作:通常使用陰性管或對照管的樣品細胞進行初步調(diào)節(jié),設(shè)置電壓的基本原則是將熒光控制在數(shù)軸的1/4范圍內(nèi),即該范圍內(nèi)的細胞都是陰性細胞,超過該范圍的都是陽性細胞。根據(jù)此原則設(shè)置電壓一般都能得到較為理想的流式圖,從而能夠得到較為準(zhǔn)確的流式結(jié)果。后續(xù)實驗組上樣分析,若發(fā)現(xiàn)無法區(qū)分陰陽性細胞還需重新調(diào)整電壓,對照管重新上樣調(diào)整。
注意:如果各實驗組的結(jié)果是根據(jù)陰性對照或同型對照的陰陽性界限得出的,那么一旦設(shè)定了對照管的電壓,后面實驗組上樣時就不能再改變電壓,否則會導(dǎo)致各實驗組之間無可比性。
對照設(shè)置
陰性對照
目的:確定細胞的非特異性熒光。細胞表面不結(jié)合熒光素也會產(chǎn)生熒光信號,流式檢測時得到的熒光信號是細胞本身的非特異性熒光和來自于細胞表面結(jié)合的熒光素的特異性熒光疊加的結(jié)果。
減一陰性對照FMO/單陽性對照(雙色)
是指在多色多通道分析時對其中某一個通道特別設(shè)置的陰性對照,多在研究不同細胞亞群表達某些表型分子、細胞因子等時應(yīng)用。
目的:精確界定不同細胞亞群各自的這一通道的陰陽性界限。因為不同細胞亞群的非特異性熒光可能存在差異,不同細胞亞群因結(jié)合不同的偶聯(lián)抗體,他們補償值可能存在差異,當(dāng)在統(tǒng)一的補償條件下同時分析時,不同細胞亞群在某一通道的陰陽性界限就可能存在差異,普通陰性對照無法進一步區(qū)分,而FMO就可以通過只缺少標(biāo)記這一通道代表的熒光素偶聯(lián)抗體來區(qū)分。
陽性對照
目的:檢測該熒光素偶聯(lián)抗體是否有效,排除假陰性結(jié)果。陽性對照并不是每次進行流式分析時都必須設(shè)置,一般在遇到以下情況時設(shè)置:
(1)初次使用的熒光素偶聯(lián)抗體;
(2)換用不同公司或相同公司不同批號的熒光素偶聯(lián)抗體;
(3)使用儲存時間較長的熒光素偶聯(lián)抗體;
以上三種情況都可能會因為各種原因?qū)е聼晒馑嘏悸?lián)抗體失效,從而無法正常標(biāo)記樣品細胞,從而得到假陰性的結(jié)果。
補償調(diào)節(jié)
因為不同熒光素被相同激光器激發(fā)后發(fā)出的波長可能會混有同波段的熒光信號,被收集后不同熒光信號之間會互相摻雜,為了區(qū)分開來就需要對各熒光信號之間進行補償調(diào)節(jié)來還原真實的熒光信號值。
熒光補償(fluorescence compensation)
*排除FL2中來自FITC的熒光信號,設(shè)置“FL2-FL1"(PE-FITC)的補償值,使FL2代表PE的熒光信號;
*排除FL1中來自PE的熒光信號,設(shè)置“FL1-FL2"(FITC-PE)的補償值,使FL1代表FITC的熒光信號,這一過程就是熒光補償。
何時需要補償調(diào)節(jié)

是否需要補償調(diào)節(jié)以及如何具體安排補償調(diào)節(jié)與實驗?zāi)康挠嘘P(guān)。
單色分析標(biāo)記一種熒光素偶聯(lián)抗體時,不需要補償調(diào)節(jié)。單色分析用FITC通道,標(biāo)記FITC偶聯(lián)的抗體,只需分析FITC通道接收的熒光信號的強弱即可,不需要分析其他通道(MFI實際值);
若是雙色或多色分析,同時標(biāo)記多種熒光素偶聯(lián)抗體,這些通道之間就需要進行補償調(diào)節(jié)。
影響補償大小的因素
主要受儀器型號(濾光片)、熒光素偶聯(lián)抗體、細胞這三方面因素的影響。
熒光通道之間的補償沒有一個固定的值。
補償?shù)木唧w方法-分組
以調(diào)節(jié)FITC通道和PE通道之間的補償為例進行介紹。
樣品細胞:小鼠脾臟細胞
抗體:FITC-抗CD8抗體、PE-抗CD4抗體
將細胞分成4份,具體標(biāo)記方法和目的見下表:
| 樣品序號 | 抗體標(biāo)記方法 | 目的 |
| 1 | 不標(biāo)記熒光素偶聯(lián)抗體 | 陰性對照 |
| 2 | 標(biāo)記FITC-抗CD8抗體 | 調(diào)節(jié)PE-FITC補償 |
| 3 | 標(biāo)記PE-抗CD4抗體 | 調(diào)節(jié)FITC-PE補償 |
| 4 | 標(biāo)記FITC-抗CD8抗體、標(biāo)記PE-抗CD4抗體 | 觀察補償調(diào)節(jié)結(jié)果 |
一份樣品細胞不標(biāo)記任何熒光素偶聯(lián)抗體,僅作為陰性對照,用于確定FITC、PE通道的陰陽性分界。
補償?shù)木唧w方法-PE-FITC補償
第二份樣品只標(biāo)記FITC-抗CD8抗體,用于調(diào)節(jié)PE-FITC補償值。
未調(diào)節(jié)補償時(PE-FITC補償值為0)的FITC-PE散點圖如下圖A所示,不僅FITC通道能夠接收到FITC熒光素發(fā)射的信號,PE通道也能夠接收到FITC熒光素發(fā)射的熒光信號,為了使FITC通道代表FITC熒光素的信號,PE通道代表PE熒光素的信號,需要將PE通道中接收到的來源于FITC熒光素的信號扣除,就是設(shè)置PE-FITC補償(PE減FITC補償)。
當(dāng)設(shè)置的PE-FITC補償越來越大時,PE接收到的來源于FITC熒光素的信號越來越少,直到如圖B所示;
如圖C所示是過度調(diào)節(jié)PE-FITC補償值的FITC-PE散點圖,F(xiàn)ITC陽性細胞群PE通道信號明顯低于FITC陰性細胞群。

第三份樣品只標(biāo)記PE-抗CD4抗體,用于調(diào)節(jié)FITC-PE補償值。
未調(diào)節(jié)補償時(FITC-PE補償值為0)的FITC-PE散點圖如下圖D所示,不僅PE通道能夠接收到PE熒光素發(fā)射的信號,F(xiàn)ITC通道也能夠接收到PE熒光素發(fā)射的熒光信號,為了使FITC通道代表FITC熒光素的信號,PE通道代表PE熒光素的信號,需要將FL1中接收到的來源于PE熒光素的信號扣除,就是設(shè)置FITC-PE補償(FITC減PE補償)。

如圖E所示的是正確調(diào)節(jié)FITC-PE補償值后的FITC-PE散點圖,此時FITC通道基本接收不到來源于PE熒光素的信號,而且PE陰陽性細胞群處于同一垂直線上。
如圖F所示是過度調(diào)節(jié)FITC-PE補償值的FITC-PE散點圖,PE陽性細胞群FITC通道信號明顯低于PE陰性細胞群。
補償?shù)木唧w方法-補償效果觀察
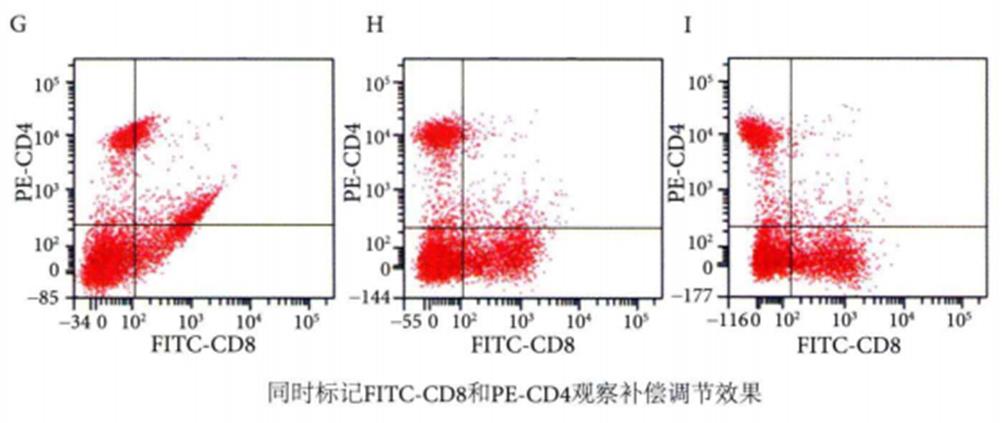
第四份樣品同時標(biāo)記FITC-CD8和PE-CD4抗體,用于觀察補償調(diào)節(jié)效果。
如圖G所示的是未調(diào)節(jié)補償時的FITC-PE散點圖,F(xiàn)ITC通道同時接收到FITC和PE熒光素發(fā)射的熒光信號;
如圖H所示的是正確調(diào)節(jié)補償后的散點圖,F(xiàn)ITC通道只接收到FITC熒光素發(fā)射的熒光信號,PE通道只接收到PE熒光素發(fā)射的熒光信號,細胞分群較為清晰。
如圖I所示的是過度調(diào)節(jié)補償后的散點圖。
調(diào)節(jié)熒光補償要求
(1)正確選擇具有代表性的熒光素偶聯(lián)抗體用于調(diào)節(jié)熒光通道之間的補償;
如需要調(diào)節(jié)FL1和FL2之間的補償,就可以選擇FITC熒光素偶聯(lián)抗體、PE熒光素偶聯(lián)抗體。
(2)選擇的兩個抗體所結(jié)合的抗原分子必須在樣品細胞中有明確的表達(表達該抗原的細胞占有較高的比例);
若陽性細胞比例太低,就無法形成明顯的細胞團,從而無法判斷補償調(diào)節(jié)是否得當(dāng);當(dāng)然比例應(yīng)不能過高,這樣不表達該抗原分子的細胞的熒光信號就可以作為陰性對照。
(3)細胞能夠高表達該抗原;
這樣才能使陽性細胞和陰性細胞明顯分群。
閾值設(shè)定
流式分析的對象是細胞,而上樣分析時的樣品中不可避免存在著或多或少的細胞碎片。雖然碎片一般都比較小,但儀器無法判斷檢測到的對象是碎片還是細胞(實驗者當(dāng)然只希望分析目的細胞),這時候就需要通過設(shè)定閾值盡可能的排除細胞碎片或其他小顆粒物質(zhì)的影響,使流式分析的對象只是細胞。
如何設(shè)定閾值(threshold)
設(shè)定閾值首先需要確定觸發(fā)通道(根據(jù)某個涉及的通道來設(shè)定),常用的是FSC通道(一般細胞碎片都比細胞小,根據(jù)FSC大小設(shè)定閾值來排除碎片比較理想)。
閾值由百分數(shù)來表示,如4%(觸發(fā)通道若是FSC就表面每檢測到100個對象就會自動排除其中FSC最小的4個對象);設(shè)定閾值只是一個經(jīng)驗值,并不是設(shè)定了閾值就可以絕對排除掉細胞碎片等等,需根據(jù)實驗實際情況調(diào)節(jié)閾值(比如制備樣本細胞不理想時間過長就可以相應(yīng)提高閾值)。
死細胞排除
樣品細胞中一般含有一定量的死細胞,通過一定的方法可以減少死細胞比例,但是去除干凈幾乎是不可能的。流式分析的目標(biāo)是活細胞,若流式分析時誤將死細胞當(dāng)成活細胞來分析,會嚴(yán)重影響流式結(jié)果。
如何減少/排除死細胞
制備階段:盡量縮短樣本制備時間,使用緩沖液等等手段保持細胞活力。
分析階段:目前有四種常見的方式區(qū)分活/死細胞,如:對角線死細胞、7AAD標(biāo)記、PE-Cy5通道非標(biāo)記陽性細胞、EMA與ViD標(biāo)記死細胞。
7AAD(7氨基放線菌素D)標(biāo)記
7AAD是一種非滲透性(無主動性)的核酸標(biāo)記染料,若細胞死亡,代謝停止導(dǎo)致質(zhì)膜受損,從而該染料能進入細胞內(nèi),一旦與細胞內(nèi)暴露的DNA結(jié)合,就和形成高強度熒光的加合物,從而被熒光通道接收(即7AAD陽性表面細胞死亡)。
7AAD發(fā)射的熒光比較集中,一般被PerCP通道接收,基本不與FITC、PE熒光重疊,可以與FITC、PE共同標(biāo)記樣本細胞(優(yōu)于PI)。
7AAD不能與PerCP或PE-Cy5偶聯(lián)的抗體共同標(biāo)記樣品細胞。標(biāo)記7AAD不需要與其他熒光素偶聯(lián)抗體同時標(biāo)記,只需要在流式上樣前加入適量7AAD于上樣管中即可。分析時,只需將PerCP通道陰性的細胞設(shè)門顯示于新的流式圖中即為正常的活細胞。
分析速度控制
流式細胞儀的液流系統(tǒng)由樣品流和鞘液流組成,雖然樣品流和鞘液流相互接觸,但是這兩個液流卻是相互獨立的,分別由兩個壓力所控制。鞘液壓力是不變的,而一般改變樣品流壓力從而調(diào)節(jié)上樣速度。
原理:為形成穩(wěn)定的層流,需保證樣品流和鞘液流的流速是相同的。改變樣品流壓力,改變樣品流的直徑。增加樣品流壓力,位于中間的樣品流的直徑就會增大,單位時間內(nèi)流過的細胞就會增加。
實際操作:流式分析對上樣速度要求不高,一般只簡單的設(shè)置幾檔分析速度供選擇,如Low、Medium和High。低速上樣時,樣品壓相對較小,樣品流直徑較小,樣品流內(nèi)的細胞位于液流正中的概率更大,分析得到的數(shù)據(jù)接近細胞的真實數(shù)據(jù),但是,耗時較長,就不適用于樣品組數(shù)較多的情況。如果樣品組數(shù)較少,時間不是主要考慮因素,則盡量低速分析。



